2023 ESMO 结直肠癌CAR-T及新辅助双免治疗新突破,为患者点燃新希望
在2023年欧洲肿瘤内科学会(ESMO)年会上,结直肠癌治疗领域的两大前沿探索——CAR-T细胞疗法与新型辅助双免疫治疗,凭借其振奋人心的早期数据,为众多患者带来了新的曙光。这些进展不仅代表了肿瘤免疫治疗的深化与创新,也预示着未来临床实践可能发生的范式转变。
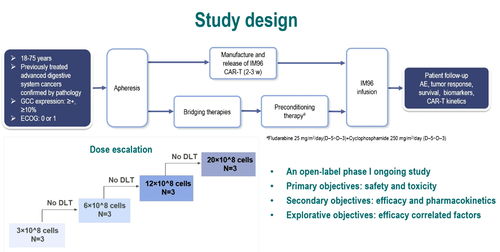
一、 CAR-T细胞疗法:攻克实体瘤的艰难一跃
长期以来,CAR-T疗法在血液肿瘤中取得了革命性成功,但其在结直肠癌等实体瘤中的应用一直面临肿瘤微环境抑制、靶点选择困难等重大挑战。本次ESMO大会上,针对结直肠癌特定靶点(如GCC、GPC3等)的CAR-T疗法早期临床研究公布了令人鼓舞的结果。
数据显示,在经过多重治疗的晚期转移性结直肠癌患者中,尤其是那些肿瘤高度表达特定抗原的患者,新型CAR-T疗法展现出了可观的客观缓解率与疾病控制率,且部分患者实现了深度缓解。研究人员通过优化CAR结构、联合使用免疫调节剂以改善T细胞在肿瘤部位的浸润与持久性,正在逐步突破实体瘤的屏障。尽管细胞因子释放综合征(CRS)等安全性问题仍需密切管理,但这些初步成功标志着CAR-T疗法在结直肠癌这一“硬骨头”上取得了实质性进展,为无药可用的晚期患者提供了全新的精准治疗选择。
二、 新辅助双免疫治疗:手术前的“围剿”策略
另一方面,在可手术的局部进展期结直肠癌领域,新辅助免疫治疗,特别是双免疫联合方案(如PD-1抑制剂联合CTLA-4抑制剂或其他新型免疫调节剂)的探索成为另一大亮点。传统的新辅助放化疗后,仍有部分患者面临复发风险。研究旨在利用手术前的时间窗,通过激活患者自身的免疫系统来清除微转移灶、缩小原发肿瘤,甚至达到病理学完全缓解(pCR),从而可能改善长期预后。
ESMO上报告的研究初步表明,在微卫星高度不稳定性(MSI-H)的结直肠癌患者中,新辅助双免治疗实现了极高的病理缓解率,部分患者甚至无需进行后续手术。更引人注目的是,在微卫星稳定(MSS)型患者——这类患者通常对单药免疫治疗不敏感——中,某些双免组合或免疫联合靶向/化疗的方案也显示出激活抗肿瘤免疫应答的潜力,显著提升了肿瘤的退缩程度。这种“术前免疫激活”策略,有望从根本上改变局部晚期结直肠癌的治疗格局,实现更佳的长期生存。
三、 挑战与未来方向
尽管前景光明,但挑战依然存在。CAR-T疗法需要解决靶向毒性、生产成本及实体瘤浸润效率等问题。新辅助双免治疗则需要精确筛选获益人群,并管理好免疫相关不良反应。未来的研究将集中于:1)发现更优的肿瘤特异性靶点;2)开发更安全高效的联合疗法方案;3)利用生物标志物(如肿瘤突变负荷、免疫微环境特征等)进行精准的患者分层。
四、 对医疗系统与辅助支持的启示
这些高度复杂的个体化治疗(如CAR-T)和精准化方案(如基于生物标志物的双免治疗)的兴起,对医疗系统提出了更高要求。从“计算机软硬件及辅助设备零售”的延伸视角看,未来癌症治疗将更加依赖于先进的辅助技术:高性能计算(HPC)用于分析基因组学数据以识别靶点与生物标志物;人工智能算法辅助影像学评估治疗反应;复杂的医疗软件系统管理治疗流程与患者数据;甚至远程监护设备用于管理患者的院外不良反应。因此,支撑精准医疗的“软硬件及辅助设备”生态系统的完善,将是这些前沿疗法能否成功惠及广大患者的关键基础设施。
2023年ESMO上关于结直肠癌的突破性报告,清晰地描绘了一个免疫治疗向更早期、更精准、更多样化迈进的时代。CAR-T疗法在实体瘤的深耕与新辅助双免治疗的开拓,如同两把利刃,正试图切开结直肠癌治疗中的顽固壁垒。尽管前路仍需跋涉,但这些探索无疑为患者点燃了强大的新希望,并预示着肿瘤治疗将与数字技术、精准诊断更深度地融合,共同迈向一个疗效更优、生存质量更高的未来。
如若转载,请注明出处:http://www.glaii.com/product/25.html
更新时间:2026-06-01 11:04:31